5.11Les bénéfices des bandes riveraines sur la qualité des plans d’eau
Les bénéfices des bandes riveraines sont nombreux. Comme nous l’avons vu précédemment, elles stabilisent les berges (figure 25), retiennent les sédiments transportés par le ruissellement de l’eau à la surface du sol (figure 26) et filtrent les nutriments en provenance des terres agricoles. Elles peuvent aussi filtrer les pesticides et les résidus d’animaux, fournir de l’ombre, des abris et de la nourriture pour les poissons et d’autres organismes aquatiques, former des habitats pour la faune terrestre, fournir des produits ayant une valeur marchande, diversifier le paysage agricole et protéger les terres agricoles contre les inondations.

Figure 25. Élevage bovin qui s’abreuve dans un cours d’eau où les signes d’érosion des berges sont multiples. Ici, on peut voir que les berges sont taillées abruptement, que le sol s’affaisse et que l’eau du cours d’eau est brunâtre (sédiments en suspension). D’autres signes d’érosion des berges incluent un déchaussement du système racinaire de la végétation sur les berges et des dépôts de plantes dans le lit du cours d’eau.
Source : Pelton (2017).

Figure 26. Deux cours d’eau qui communiquent en Malaisie. Celui de gauche, caractérisé par une eau brunâtre (riche en sédiments), provient d’un bassin versant dans lequel l’industrie n’a pas conservé des bandes riveraines lors des activités de récolte. Celui de droite, caractérisé par une eau limpide, provient d’un bassin dans lequel l’industrie a maintenu plusieurs bandes riveraines.
Source : Forests Monitor.
Les bandes riveraines limitent l’apport de sédiments de six façons :
- elles éloignent des plans d’eau les activités pouvant générer des sédiments;
- elles piègent les sédiments contenus dans le ruissellement de surface (effet de barrière physique);
- elles ralentissent la vitesse du ruissellement de surface de façon à permettre aux sédiments de se redéposer à la surface du sol et à l’eau de se purifier;
- elles stabilisent les berges, diminuant ainsi l’érosion du lit des cours d’eau;
- elles réduisent les débits des cours d’eau en interceptant et en utilisant une bonne portion des précipitations, limitant aussi l’érosion du lit des cours d’eau; et
- elles rejettent des débris ligneux directement dans le chenal des cours d’eau, piégeant des quantités considérables de sédiments, du moins temporairement.
Dans le cas du processus 3), cela inclut également les sédiments qui étaient en suspension dans le cours d’eau, mais qui ont été transportés jusque dans la bande riveraine lors d’une inondation.
Par exemple, on peut observer à la figure 27 que la présence de bandes riveraines n’a pas nécessairement d’impact sur le débit de cours d’eau en Malaisie. Toutefois, les bandes riveraines diminuent significativement les concentrations de sédiments en suspension par rapport au cours d’eau qui n’avait pas de bandes de protection. Les mécanismes de piégeage des sédiments n’ont pas été mesurés, mais on peut penser que plusieurs des mécanismes identifiés ci-dessus jouent un rôle important dans la diminution de la charge de sédiments dans l’eau.
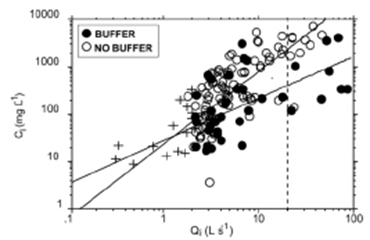
Figure 27. Concentrations de sédiments en suspension (Ci, en mg par litre) selon les débits (Qi, litre par seconde) de deux cours d’eau en Asie, l’un en présence de bandes riveraines (BUFFER, cercles fermés) et l’autre en absence de bandes riveraines (NO BUFFER, cercles ouverts). Les deux lignes sont les lignes de régression des deux bases de données, alors que le symbole « + » représente les données à l’étiage.
Source : Ziegler et al. (2006).
La capacité d’une bande riveraine à piéger les sédiments dépend de sa largeur. En général, plus la bande riveraine est large et plus sa capacité de piégeage est grande. C’est ce qu’on peut observer à la figure 28. On observe cependant qu’à une largeur de 25 m et plus, les bénéfices d’augmenter la largeur d’une bande riveraine sont plus petits (voir Peterjohn et Correll [1984], figure 28).
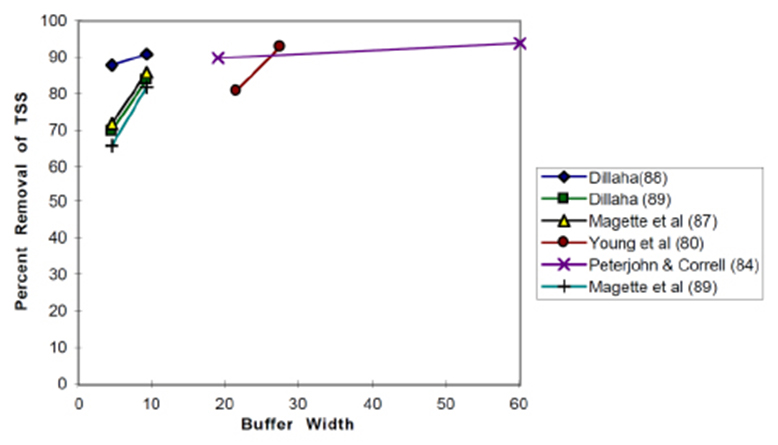
Figure 28. Pourcentage de sédiments en suspension piégés (Percent Removal of TSS) selon la largeur (en mètres) de la bande riveraine (Buffer Width). Les lignes de différentes couleurs représentent diverses études sous des conditions variées.
Source : Wenger (1999).
La pente est également un facteur important à considérer lors de la construction ou de la conservation d’une bande riveraine. Généralement, plus la pente est forte, moins la bande riveraine est efficace à piéger les sédiments contenus dans les eaux de ruissellement (figure 29). Logiquement, on peut penser qu’il faut augmenter la largeur de la bande pour augmenter son efficacité. C’est ce que la figure 29 suggère, c’est-à-dire que le piégeage des sédiments est supérieur pour la bande de 9,1 mètres de largeur, autant pour les données recueillies en 1988 qu’en 1989. Toutefois, on observe que cette bande de 9,1 mètres perd autant d’efficacité à piéger les sédiments que la bande de 4,6 mètres lorsque la pente augmente de 10 à 15 %. Selon Fennesy et Cronk (1997), le plus grand problème lorsque vient le temps d’évaluer la largeur de bande requise pour protéger le cours d’eau adjacent provient du fait que les études qui cherchent à faire des recommandations quant à la largeur minimale requise proposent des chiffres qui sont le sous-produit d’un dispositif expérimental restreint et sous des conditions qui ne représentent pas nécessairement les conditions d’autres sites. Idéalement, il faudrait que ces chiffres soient dérivés d’études qui répondent spécifiquement aux conditions de site, mais ce scénario est impossible dans la pratique. Malgré les nombreuses études, nous en sommes encore à estimer la largeur requise. Il y aura donc toujours un risque associé à la conception d’une bande riveraine – parfois elle donnera de bons résultats et parfois elle donnera de mauvais résultats. Il faut dire également que les résultats varieront selon les objectifs visés. Une bande riveraine peut s’avérer efficace pour piéger les sédiments, mais moins efficace pour séquestrer l’azote et le phosphore. L’inverse est également possible. Une bande peut même être efficace à séquestrer un nutriment, mais pas un autre. Nous étudierons cette question un peu plus loin dans le module.
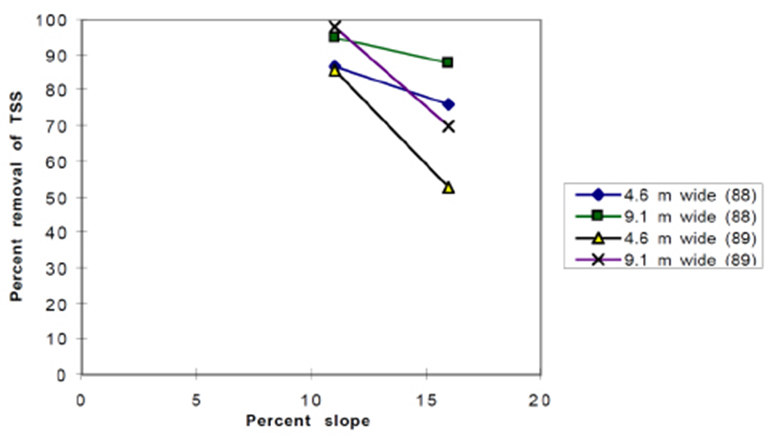
Figure 29. Pourcentage de sédiments en suspension piégés (Percent removal of TSS) selon deux largeurs (Wide) de bandes riveraines (4,6 et 9,1 mètres) et la pente du terrain (Percent slope). Les lignes en bleu et vert représentent les données recueillies en 1988, et en jaune et mauve les données recueillies en 1989.
Source : Wenger (1999).
Les bandes riveraines ne peuvent pas servir à piéger les sédiments dans le cas de ravinement (ou érosion en ravin, figure 30) parce que la vitesse d’écoulement de l’eau étant trop rapide, l’eau et les sédiments ne sont canalisés que dans quelques chenaux. La situation est semblable lors de périodes de fortes pluies, puisque les eaux de ruissellement circulent trop rapidement et que les bandes ne les ralentissent pas suffisamment pour permettre aux sédiments, notamment les particules sableuses, de se déposer sur le sol avant d’atteindre les plans d’eau. De plus, il faudra que la bande ralentisse significativement les eaux de ruissellement pour permettre aux limons et aux argiles de se déposer sur le sol, ce qui est rarissime. Ces particules sont plus petites que les particules sableuses et prennent plus de temps pour sédimenter. En fait, les bandes riveraines les plus efficaces peuvent piéger une bonne portion des limons, mais les argiles sont rarement piégées en raison de temps de sédimentation très longs.
La détérioration de la qualité des plans d’eau par les nutriments comme l’azote et le phosphore est courante en milieu agricole. Les eaux de ruissellement contribuent à des nutriments en transportant de la matière organique (incluant les débris végétaux et les fèces des animaux) et des particules de sol, lesquelles contiennent de l’azote et du phosphore. Les programmes de fertilisation des fermes contribuent aussi à de grandes quantités de nutriments aux plans d’eau par la pollution diffuse. Ce sont les nutriments en excès à la demande des cultures, appliqués sous la forme de fertilisants chimiques, de composts ou de fumiers, qui parviennent éventuellement aux plans d’eau par l’écoulement hypodermique et la nappe phréatique. Enfin, il y a d’autres sources de nutriments qui ne sont pas d’origine agricole. Les drains de fosses septiques (figure 31), les égouts défectueux (fuites) et la fertilisation des gazons peuvent contribuer à des quantités considérables de nutriments aux eaux de surface.
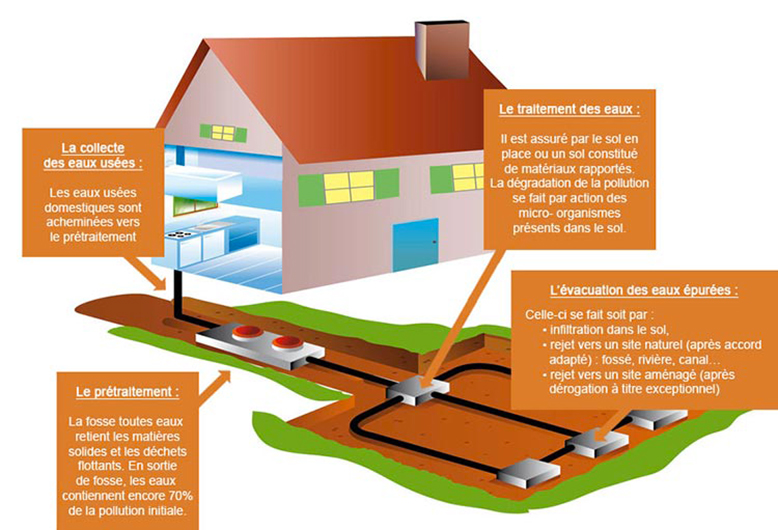
Figure 31. Schéma du fonctionnement d’un assainissement individuel (non collectif) des eaux usées.
Source : https://www.mg-assainissement.com/entreprise-assainissement-06-fosse-septique-cagnes-sur-mer.html
Généralement, la fertilisation des cultures et l’élevage sont parmi les plus grandes sources de pollution des eaux de surface par l’azote et le phosphore. On peut le constater pour le bassin de drainage d’Albemarle-Pamlico en Caroline du Nord et en Virginie, aux États-Unis (figure 32). Les apports en azote et en phosphore dans les précipitations sont négligeables, alors que ceux en provenance de sources ponctuelles (ex. effluents d’usine – eaux usées) sont inférieurs à ceux provenant de l’agriculture (figure 32).
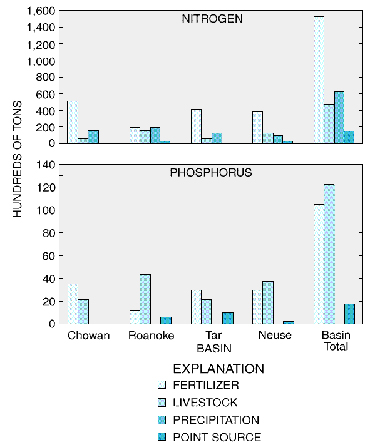
Figure 32. Apport d’azote et de phosphore en centaines de tonnes (hundreds of tons) par type de source (fertilisants – fertilizer; élevage – livestock; précipitation – precipitation; sources ponctuelles comme les effluents d’usines – point source) dans le bassin de drainage Albemarle-Pamlico en Caroline du Nord et en Virginie, États-Unis, entre 1992 et 1995. L’axe des x compte quatre sous-bassins (Chowan, Roanoke, Tar et Neuse) ainsi que le total du grand bassin (Basin Total).
Source : Spruill et al. (1998).
L’apport d’azote et de phosphore dans les cours d’eau constitue une problématique environnementale importante. Une surcharge de ces nutriments dans les eaux de surface cause l’eutrophisation. Le phénomène est simple. Les algues prolifèrent au fur et à mesure que le plan d’eau se charge en azote et en phosphore. Au début du processus, l’eau reste bien oxygénée. Toutefois, l’activité des microorganismes tend à augmenter avec le temps parce que la quantité d’algues en sénescence tend aussi à croître. La décomposition des algues sénescentes par les microorganismes a pour effet d’appauvrir l’eau en oxygène (demande biochimique en oxygène élevée). Dans les cas les plus sévères, les poissons sont asphyxiés parce que le plan d’eau atteint un état d’anoxie (stade eutrophe, figure 33).
Les bandes riveraines sont particulièrement efficaces pour séquestrer le phosphore dans les eaux de ruissellement en provenance des terres agricoles. Tout comme les sédiments en suspension, l’efficacité des bandes dépend de leurs largeurs – plus la bande est large et plus la séquestration du phosphore sera grande (figure 34). Une seule étude suggère un patron contraire, celle de Dillaha et al. en 1988. Toutefois, en 1989, le même dispositif montre que la bande riveraine plus large a séquestré davantage de phosphore. Le mécanisme de piégeage du phosphore est le même que celui des sédiments, puisque la majorité du phosphore séquestré par les bandes riveraines l’est sous forme particulaire (forme solide).
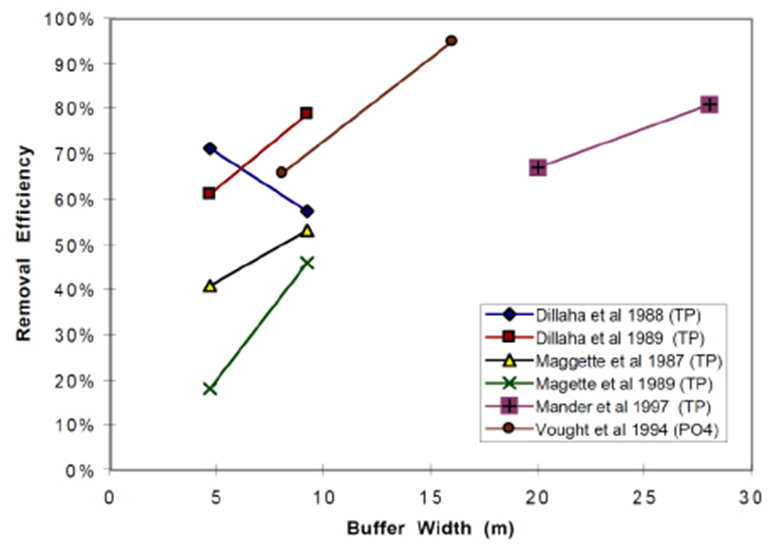
Figure 34. Pourcentage de sédiments en suspension piégés (Removal Efficiency) selon la largeur (en mètres) de la bande riveraine (Buffer Width). Les lignes de différentes couleurs représentent diverses études sous des conditions variées.
Source : Wenger (1999).
Le phosphore dissous (ion phosphate, PO43-), quant à lui, est moins facilement saisissable. Il est principalement prélevé par la végétation de la bande riveraine et retenu à la surface des particules (organiques et minérales) de sol. Il peut aussi précipiter avec les métaux pour former des complexes chimiques stables (ex. complexes d’aluminium et de phosphore). À long terme, toutefois, ces mécanismes deviennent moins actifs. Notamment, le prélèvement du phosphore dépendra des taux de croissance et de la vigueur des arbres. Une bande riveraine vieillissante aura des taux de prélèvement du phosphore plus faibles qu’une bande en pleine croissance. De plus, les surfaces des particules de sol se chargent au fur et à mesure que le phosphore est mobilisé dans les eaux de ruissellement. Lorsque ces mécanismes ralentissent, la bande riveraine perd vraisemblablement son efficacité à séquestrer le phosphore. Dans l’ensemble, on peut conclure que les bandes riveraines sont utiles pour piéger le phosphore particulaire, mais qu’elles ne le sont pas pour séquestrer le phosphore dissous.
Au contraire, les bandes riveraines sont extrêmement efficaces à séquestrer l’azote dissous (ions nitrate [NO3–] et l’ammonium [NH4+]), et ce, à long terme. Toutefois, les mécanismes qui permettent la séquestration de l’azote à long terme sont encore mal compris. Le prélèvement par la végétation de la bande est, sans équivoque, un mécanisme de séquestration important de l’azote dissous (figure 35). Certaines espèces d’arbres auront une préférence pour l’ion nitrate (espèces feuillues), d’autres pour l’ion ammonium (espèces résineuses). Mais comme pour le phosphore dissous, ce mécanisme s’amenuise lorsque la productivité de la bande diminue avec l’âge. À plus long terme, la séquestration de l’azote est liée au processus de dénitrification (c’est-à-dire à une déoxygénation par l’action des bactéries spécifiques de l’ion nitrate en molécules gazeuses, soit le NO, suivi de N2O et enfin de N3, figure 35). L’ion nitrate, en provenance des terres agricoles, est ainsi réduit en gaz dans la bande riveraine et ceux-ci sont perdus de façon permanente par volatilisation. Ce mécanisme est un puits actif spécifiquement dans la bande riveraine, parce que c’est elle qui crée les sols anoxiques (milieu réducteur) nécessaires à la dénitrification. Certains chercheurs proposent que l’ion nitrate soit prélevé par la végétation et redistribué à la surface du sol avant d’être réduit par les bactéries dénitrifiantes. Si le carbone n’est pas limitant pour les bactéries, ce mécanisme de séquestration de l’azote peut vraisemblablement être très élevé dans les bandes riveraines les plus humides.
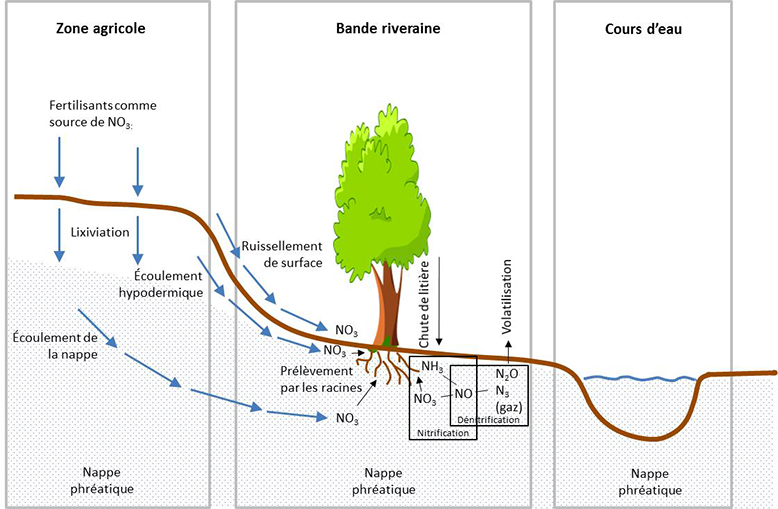
Figure 35. Schématisation des mécanismes de séquestration de l’azote soluble (NO3–) dans les bandes riveraines.
Source : Adapté de United State Department of Agriculture – Forest Service.
Les études ont montré un taux élevé et généralisé de séquestration de l’azote soluble par les bandes riveraines (tableau 4). Des concentrations de l’ion nitrate supérieures à 10 milligrammes par litre peuvent être problématique pour la consommation et l’écologie des plans d’eau (ex. eutrophisation). Notez que pour toutes les études, ce seuil n’est pas dépassé en présence d’une bande de protection des plans d’eau.
Tableau 4. Taux de séquestration et concentration de l’ion nitrate dans les eaux de la nappe phréatique ayant traversé une bande riveraine.
| Largeur de la bande | Taux de séquestration (%) – comparaison des eaux de la nappe phréatique en amont et en aval de la bande | Concentration de l’ion nitrate en aval de la bande (en milligrammes par litre) | |
|---|---|---|---|
| Osborne et Kovacic (1993) | 16 | 96 | <1,0 |
| Haycock et Pinay (1994) | 16 | 84 | Non détectable |
| Haycock et Pinay (1994) | 20 | 99 | Non détectable |
| Mander et al. (1997) | 20 | 81 | Non détectable |
| Mander et al. (1997) | 28 | 80 | Non détectable |
| Hubbard (1997) | 30 | 78 | 9,0 |
| Hanson et al. (1994) | 31 | 94 | <1,0 |
| Osborne et Kovacic (1993) | 39 | 95 | 0,5 |
| Jordan et al. (1993) | 60 | 95 | 0,4 |
| Lowrance (1992) | 60 | 94 | 0,81 |
Source : Adapté de Wenger (1999).
L’ion nitrate parvient jusqu’aux eaux de surface par l’entremise des eaux souterraines en tout temps et l’écoulement hypodermique en périodes arrosées. Puisque l’ion nitrate est très soluble et qu’il se déplace rapidement dans les eaux souterraines, la séquestration de celui-ci par la bande riveraine dépend largement du contact entre les eaux souterraines et la zone racinaire de la bande. De ce fait, dans le cas d’une nappe qui s’écoule à travers les couches superficielles de sol, le prélèvement de l’ion nitrate sera accru parce que la nappe doit nécessairement passer par la zone racinaire (figure 36). Les taux de séquestration de l’ion nitrate dépendent aussi du temps de résidence de l’eau dans la zone racinaire, laquelle est fonction de sa vitesse d’écoulement. Plus le temps de résidence est long et plus les taux de séquestration seront élevés.
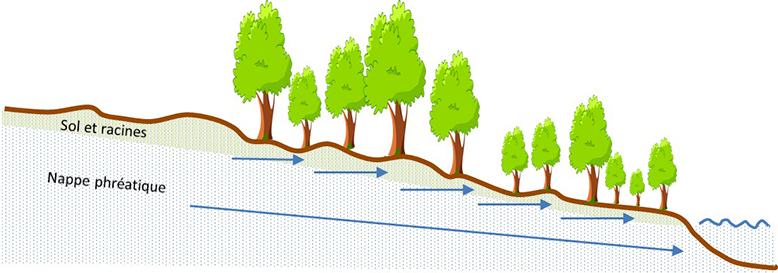
Figure 36. Écoulement des eaux souterraines à travers les couches superficielles de sol d’une bande riveraine.
Dans le cas d’une nappe qui circule dans les couches plus profondes du sol, une large portion de la nappe s’écoulera sous la zone racinaire de la bande riveraine. Ainsi, même si le temps de résidence de la nappe est long, les racines de la bande sont inefficaces pour prélever l’ion nitrate, lequel se trouve trop en profondeur dans les eaux de la nappe (figure 37).
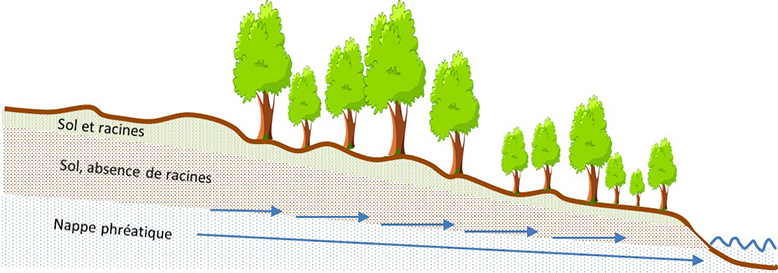
Figure 37. Écoulement des eaux souterraines à travers les couches profondes de sol d’une bande riveraine.
Malheureusement, il y a une relation inverse entre la dénitrification et la séquestration du phosphore dans les bandes riveraines. Cela peut se traduire par un piégeage du phosphore et une libération de l’azote, ou vice-versa. L’explication est d’ordre chimique. Dans les sols anoxiques, propices à la dénitrification et à la volatilisation de molécules gazeuses comme N2O et N2, la réduction (gain d’un électron et perte d’une charge) des oxydes et des hydroxydes de fer est favorisée :
Fe3+ + e- ⟹ Fe2+
Cette réaction favorise la mobilisation du fer ferreux ou fer(II) (Fe2+), beaucoup plus soluble que le fer ferrique ou fer(III) (Fe3+), et du phosphore sous la forme de l’ion phosphate (figure 38). Ainsi, pendant que l’ion nitrate est transformé et évacué de façon permanente sous la forme gazeuse, l’ion phosphate est solubilisé davantage. C’est pour cette raison que la plupart des bandes riveraines sont très efficaces à limiter la migration de l’azote soluble vers les plans d’eau, mais beaucoup moins pour limiter le transport du phosphore soluble.
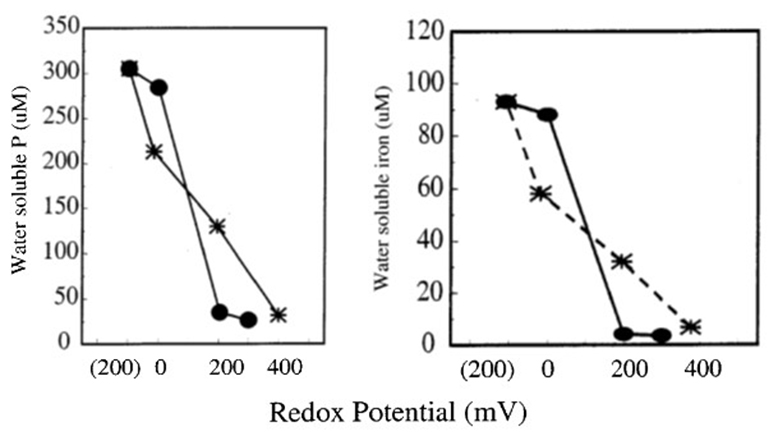
Figure 38. Solubilité (Water soluble) du fer (iron) et du phosphore (P) en micromoles (µM) selon le potentiel d’oxydoréduction (Redox Potential [mV]) d’un sol organique. Une valeur mV négative indique un potentiel de réduction et une valeur positive indique un potentiel d’oxydation.
Source : Adapté de Ann et al. (2000).

