3.4La biodisponibilité du phosphore et de l’aluminium dans les sols tropicaux
Comme discuté en début de module, les sols tropicaux comme les oxisols et les ultisols sont acides. Ce niveau d’acidité cause des ennuis aux producteurs parce que le phosphore n’est pas biodisponible à des pH trop bas. Le phosphore est rendu disponible par l’altération des minéraux du sol. Le minéral qui en contient le plus est l’apatite (Ca5(PO4)3) (figure 24).

Figure 24. Cristaux d’apatite dans un bloc de quartz.
Sous l’action de l’eau et de l’acide carbonique (H2CO3) à des pH de sol tirant vers la neutralité, l’apatite est dissoute et le phosphore est relâché sous la forme de l’ion (anion) hydrogénophosphate (HPO42-). Des ions (cations) de calcium (Ca2+) sont aussi relâchés et de l’eau (H2O) est produite :
Ca5(PO4)3 + 4H2CO3 ? 5Ca2+ + 2HPO42- + 4HCO3– + H2O
Sous des conditions plus acides comme ceux des oxisols et des ultisols, l’ion dihydrogénophosphate (H2PO4-), chargé négativement, peut être retenu par les surfaces des hydroxydes de fer (Fe) et d’aluminium (Al), lesquelles sont chargées positivement (surface <Fe3+) :
Surface<Fe3+ + H2PO4– ? surface<FeH2PO42+
Ce même ion peut aussi réagir chimiquement avec le fer et l’aluminium sous les conditions acides pour former de nouveaux minéraux. Peu importe si les ions phosphate sont retenus sur les surfaces d’échange ou encore pris en pince par la néoformation d’un minéral, ces processus chimiques agissent comme un réel puits de phosphore, le rendant indisponible pour la végétation, notamment les cultures.
Dans ce sens, la disponibilité du phosphore dépend en grande partie du statut acide-base du sol (figure 25). À des pH entre 3 et 4, le phosphore est principalement retenu par le fer, alors qu’à des pH entre 4 et 5, le phosphore est retenu par l’aluminium. C’est dans la plage de 6 et 7 que le phosphore atteint une biodisponibilité optimale, car le phosphore forme un précipité avec le calcium entre des pH de 7 et 9, soit le début de conditions d’alcalinité.
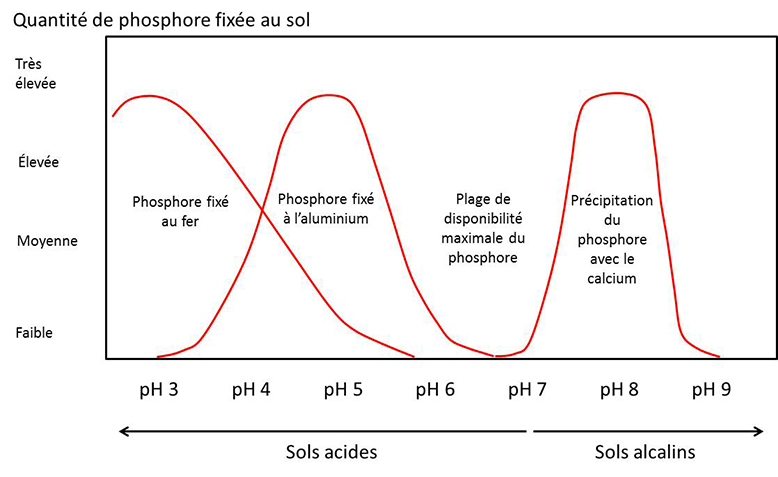
Figure 25. Relation entre la biodisponibilité du phosphore et le pH du sol.
Source : Adapté de https://crystalgreen.com/agriculture/
À des valeurs de pH qui oscillent entre 3 et 4, la solubilité de l’aluminium et du fer est élevée. Par exemple, la figure 26 montre clairement que la concentration en aluminium (Al) dans la solution de sol augmente de façon importante avec une diminution du pH (donc une hausse de l’acidité).
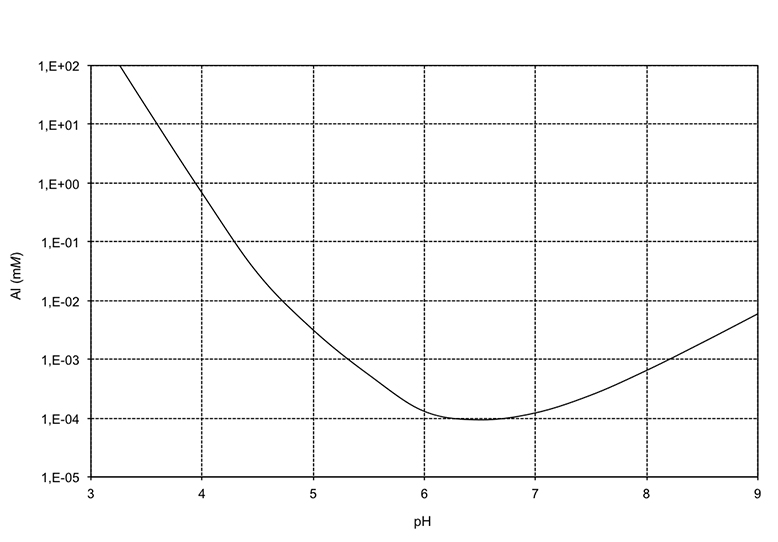
Figure 26. Solubilité de l’aluminium (Al) en millimoles (mM) selon le pH.
Source : Bélanger et al. (1999).
L’aluminium peut devenir phytotoxique lorsqu’il atteint de trop fortes concentrations dans la solution pour deux raisons : (1) il crée des dommages irréversibles aux racines en interagissant avec les biomolécules les plus sensibles, et (2) il crée une interférence antagoniste sur le prélèvement de nutriments cationiques comme le calcium (Ca2+) ou le magnésium (Mg2+).
En incorporant des arbres dans le paysage agricole, il est possible d’augmenter la disponibilité en phosphore dans les sols de deux façons. La première est de relâcher du phosphore par la décomposition de la litière des arbres. La deuxième est de produire des acides organiques qui se lient (chélates) au fer et à l’aluminium, réduisant ainsi leur potentiel de fixer le phosphore et (ou) de former des précipités. Par le fait même, les complexes qui se forment ne sont pas assimilables par les plantes étant donné leurs poids moléculaires élevés. Ceci a pour effet de diminuer la phytotoxicité de l’aluminium, tel qu’observé par la relation négative entre la quantité d’aluminium qui n’est pas complexé aux acides organiques (c’est-à-dire l’aluminium libre ou monomérique) et le rendement des cultures (figure 27).
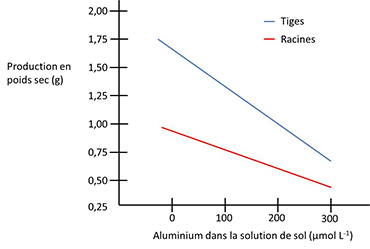
Figure 27. Relation entre les concentrations de l’aluminium monomérique dans la solution (culture hydroponique) et la biomasse (sèche) de tiges et de racines de maïs produite.
Source : Adapté de Fernandes Batista et al. (2013).
Toutefois, contrairement à l’azote, les techniques agroforestières sont souvent insuffisantes pour mitiger complètement les déficiences en phosphore dans les sols tropicaux acides et les producteurs doivent souvent recourir au chaulage et à la fertilisation avec le superphosphate triple (TSP) pour remédier aux limitations causées par ce nutriment.
En ce qui a trait au chaulage du sol, il s’agit d’ajouter de la chaux agricole (carbonate de calcium [CaCO3] broyé finement), ce qui favorise les réactions suivantes en présence d’eau.
La chaux est dissoute lentement par l’eau pour produire des ions Ca2+ et OH– :
CaCO3 + H2O (sol) ? Ca2+ + 2OH– + CO2 (gaz)
Les ions Ca2+ produits lors de la dissolution de la chaux délogent ensuite les ions Al3+ et H+ sur les surfaces d’échange du sol :
2Ca2+ + soil< Al3+ ? soil<Ca2+ + Al3+ + soil< H+ ? soil<Ca2+ + H+
Les ions OH– produits lors de la dissolution de la chaux réagissent avec les ions Al3+ pour former des précipités de Al(OH)3 :
Al3+ + 3OH– ? Al(OH)3 (solide)
Les ions OH- produits lors de la dissolution de la chaux réagissent avec les ions H+ pour former de l’eau (autoprotéolyse) :
H+ + OH– ? H2O
Par l’entremise de réactions avec OH–, le chaulage élimine l’acidité du sol en consommant H+. Le chaulage fait donc augmenter le pH du sol, ce qui a des impacts positifs sur la disponibilité du phosphore. La hausse du pH mitige également la phytotoxicité de l’aluminium.